Thomas tiene cincuenta y dos años. Come bio, hace deporte tres veces por semana, no fuma, bebe con moderación. Desde hace dos años, toma un complemento antioxidante comprado en farmacia: vitamina C, vitamina E, betacaroteno, el trío clásico vendido a millones de ejemplares con la promesa de « luchar contra el envejecimiento ». Dos años después, Thomas sigue cansado. Sus articulaciones duelen al despertar. Su piel ha perdido brillo. Sus análisis de sangre clásicos son normales. Y cuando le prescribí un balance oxidativo completo, el resultado fue un choque: su SOD eritrocitaria se había derrumbado, su glutatión peroxidasa era baja, su selenio estaba a 65 µg/L (objetivo > 100), y su glutatión reducido estaba en el piso. Thomas llevaba dos años tomando antioxidantes, y sin embargo su organismo estaba en pleno estrés oxidativo.
La paradoja de Thomas ilustra un error fundamental que el Pr Vincent Castronovo, MD PhD, profesor de la universidad de Lieja y docente del DU de Micronutrición, desmonta en su curso sobre energía y estrés oxidativo. Tomar antioxidantes exógenos cuando las defensas endógenas están derrumbadas es como repintar una fachada cuyas fundaciones se desmoronan. El problema de Thomas no era una falta de vitamina C. Era un déficit en selenio, zinc y cofactores del glutatión que impedía que sus enzimas antioxidantes funcionaran.
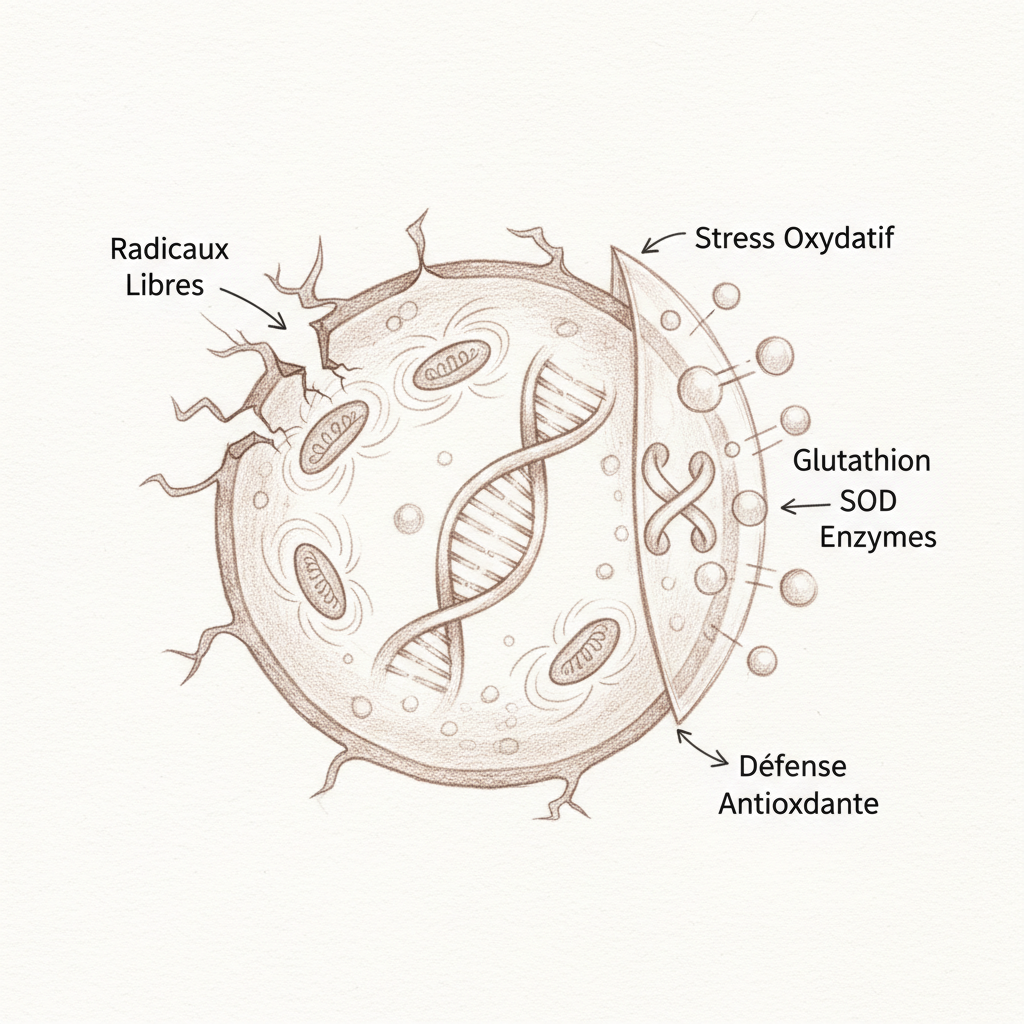
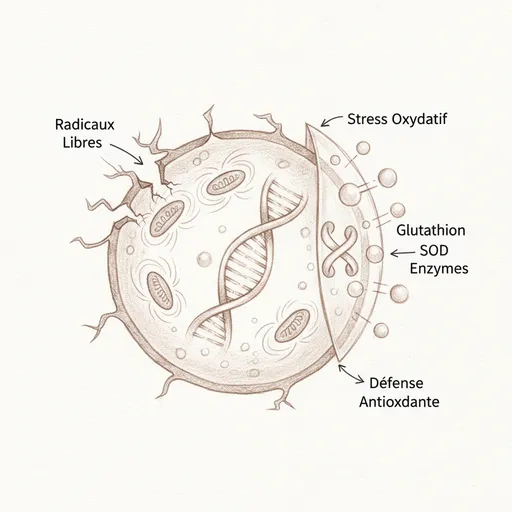
« Nuestro organismo se defiende de la actividad destructiva de los radicales libres gracias a sistemas antioxidantes seguros y eficaces. Si la producción de radicales libres aumenta más allá de las capacidades de defensa, o si estas últimas son defectuosas, entonces los radicales libres podrán atacar nuestras propias moléculas. » Pr Vincent Castronovo, DU MAPS 2020, curso #13 “Energía y Estrés Oxidativo”1
Tus células queman 50 kilos de ATP al día
Para entender el estrés oxidativo, primero hay que entender de dónde viene la energía de tus células. Un individuo quema aproximadamente 50 kilos de ATP al día2. Cincuenta kilos. El ATP (adenosina trifosfato) es la moneda energética universal de la vida. Cada contracción muscular, cada latido del corazón, cada transmisión nerviosa, cada síntesis de proteína consume ATP.
Este ATP se produce principalmente en las mitocondrias, orgánulos celulares que son en realidad antiguas bacterias. Hace 1,6 mil millones de años, inventaron un sistema bioquímico que permitía utilizar las propiedades inicialmente tóxicas del oxígeno: la respiración celular. Este invento multiplicó la producción de energía por un factor de 18 en comparación con la fermentación anaeróbica.
Poseemos aproximadamente 3 cuatrillones de mitocondrias (3 000 000 000 000 000)3. Tres mil millones de millones. El corazón, el cerebro, el hígado y los músculos son los órganos más ricos en mitocondrias, porque son los que consumen más energía. La mitocondria posee su propio ADN (16 569 pares de bases, transmitido exclusivamente por la madre), sus propios ribosomas y su propia maquinaria de síntesis de proteínas. Es literalmente un organismo dentro del organismo.
La cadena de transporte de electrones, alojada en la membrana interna de la mitocondria, es el mecanismo central de la producción de ATP. Los electrones extraídos de los nutrientes (glucosa a través de la glucólisis, ácidos grasos a través de la betaoxidación) son transportados por el NAD (cuyo precursor es la vitamina B3) y el FAD (cuyo precursor es la vitamina B2) a través de una serie de complejos proteicos (complejos I a V)4. La energía liberada por esta transferencia sirve para bombear protones (H+) en el espacio intermembranario, creando un gradiente que hace girar la ATP sintasa (complejo V), la turbina molecular que ensambla el ATP.
La coenzima Q10 es el transportador de electrones entre el complejo I y el complejo II. El citocromo C toma el relevo cuando el electrón ha perdido parte de su energía. El hierro y el cobre son cofactores esenciales de los complejos I, II, III y IV. El artículo sobre envejecimiento celular detalla en profundidad el vínculo entre mitocondrias, energía y envejecimiento.
10 % de los electrones caen: la fuente del estrés oxidativo
Este es el punto crucial. La cadena de transporte de electrones no es perfecta. Aproximadamente 10 % de los electrones altamente energéticos « caen » de la cadena de transporte antes de llegar al oxígeno de forma controlada5. Estos electrones fugitivos encuentran el oxígeno molecular (O2) de forma no controlada y lo transforman en radical superóxido (O2•-), una especie reactiva de oxígeno (ROS) extremadamente inestable y tóxica.
Este es el precio que pagamos por respirar. El oxígeno es a la vez nuestro combustible y nuestro veneno. Cada respiración produce energía Y radicales libres. Es un pacto faustiano que la evolución aceptó hace 1,6 mil millones de años, a cambio de la potencia energética de la respiración aeróbica.
Los radicales libres no provienen solo de las mitocondrias. Se distinguen tres fuentes endógenas principales: la mitocondria (fuente mayor), la inflamación (activación de macrófagos y neutrófilos que producen ROS para matar patógenos) y la detoxicación hepática (la fase I de los citocromos P450 genera intermediarios reactivos)6. Las fuentes exógenas incluyen los UV, las radiaciones ionizantes, el tabaco, el alcohol, los contaminantes atmosféricos, los pesticidas y los xenobióticos.
Los objetivos de los radicales libres son tres categorías de moléculas biológicas. Las proteínas se desnaturalizan por oxidación de sus grupos tiol, lo que altera las enzimas y los receptores. Los lípidos, en particular los ácidos grasos poliinsaturados de las membranas celulares, sufren una peroxidación en cadena que rigidifica las membranas y perturba el funcionamiento de las mitocondrias (cuya membrana interna es rica en DHA)7. El ADN sufre roturas de una y doble cadena, modificaciones de bases (8-OHdG) y mutaciones que se acumulan con la edad y favorecen la carcinogénesis.
La tríada de defensa: SOD, GPx, catalasa
Nuestro organismo no está sin defensa. El sistema de defensa antioxidante endógena es de una sofisticación notable, organizado en tres líneas8.
La primera línea es la superóxido dismutasa (SOD). Transforma el radical superóxido (O2•-) en peróxido de hidrógeno (H2O2). Existen tres formas de SOD: la SOD1 (cobre-zinc), localizada en el citoplasma, la SOD2 (manganeso), localizada en la matriz mitocondrial, y la SOD3 (cobre-zinc), extracelular. El cobre, el zinc y el manganeso son, por lo tanto, cofactores directos de la primera línea de defensa antioxidante. Una carencia en zinc debilita directamente esta primera barrera.
La segunda línea es la glutatión peroxidasa (GPx). Transforma el peróxido de hidrógeno (H2O2) en agua (H2O). Su cofactor esencial es el selenio. Sin selenio, la GPx no funciona, y el H2O2 se acumula en la célula. El glutatión reducido (GSH) es el donador de electrones de la GPx: se oxida en glutatión disulfuro (GSSG) durante la reacción, luego se regenera por la glutatión reductasa (que requiere NADPH, él mismo proveniente de la vía de los pentosas fosfato)9. La catalasa, presente principalmente en los peroxisomas hepáticos, constituye una vía complementaria de degradación del H2O2.
La catástrofe ocurre cuando el H2O2 no se neutraliza. En presencia de hierro ferroso (Fe2+) o cobre (Cu+), el H2O2 se transforma espontáneamente en radical hidroxilo (OH•) por la reacción de Fenton. Y aquí es donde todo cambia: no tenemos ningún sistema enzimático capaz de neutralizar el radical hidroxilo10. El radical OH• es el más destructivo de todos los radicales libres. Es una bomba molecular que ataca todo lo que encuentra en un radio de algunos nanómetros. Cuando se produce, el daño es inevitable.
Por eso el exceso de hierro libre es tan peligroso. Por eso la ferritina debe vigilarse no solo para la anemia (ferritina baja) sino también para la sobrecarga (ferritina > 200 en la mujer, > 300 en el hombre). Por eso el exceso de cobre libre es pro-oxidante y el ratio cobre/zinc debe medirse. Y por eso el selenio es probablemente el micronutriente antioxidante más importante y más subestimado.
El selenio: el guardián que 30 % de los franceses no tienen
Una cifra alarmante: 30 % de los franceses tienen déficit de selenio11. Treinta por ciento. Es uno de cada tres franceses cuya glutatión peroxidasa no puede funcionar correctamente, cuyo H2O2 se acumula, y cuyo riesgo de reacción de Fenton aumenta.
El estudio de Brooks et al. (2001) citado en el curso es particularmente sorprendente. Publicado en el Journal of Urology, muestra que un nivel plasmático de selenio bajo antes del diagnóstico se asocia con un riesgo 4 a 5 veces mayor de cáncer de próstata12. Los hombres del cuartil más bajo de selenio tenían un riesgo multiplicado por cinco respecto a aquellos del cuartil más elevado. El selenio disminuye significativamente con la edad, lo que hace la suplementación particularmente importante en hombres mayores de 50 años.
El selenio no actúa solo. Es cofactor no solo de la GPx sino también de las tiorredoxina reductasas y de las iodotironina desiodasas (las enzimas que convierten la T4 en T3 activa en la tiroides). Una carencia en selenio afecta, por lo tanto, simultáneamente la defensa antioxidante Y la función tiroidea, lo que explica la frecuencia de la asociación Hashimoto + estrés oxidativo.
El ácido alfa-lipoico: el antioxidante universal
Un antioxidante merece el título de « primer antioxidante de las mitocondrias » y de « antioxidante universal »: el ácido alfa-lipoico13.
El ácido alfa-lipoico posee propiedades únicas. Es a la vez hidrosoluble y liposoluble, lo que le permite actuar en todos los compartimentos celulares. Cruza la barrera hematoencefálica (protegiendo el sistema nervioso central). Neutraliza muchos radicales libres diferentes. Y lo más importante, regenera todos los otros antioxidantes después de que han sido oxidados: vitamina C, vitamina E, glutatión, tiorredoxina y ubiquinona (CoQ10). En su forma reducida (ácido dihidrolipoico), es el reciclador principal de la red antioxidante.
Es también el primer cofactor de la piruvato descarboxilasa, el complejo enzimático que permite la entrada del piruvato en la mitocondria (con la vitamina B1). Sin ácido alfa-lipoico, la glucosa no puede transformarse en energía mitocondrial. Por eso es particularmente estudiado en la diabetes tipo 2 y la neuropatía diabética.
Los antioxidantes exógenos: complementos, no sustitutos
Los antioxidantes exógenos son complementos de las defensas endógenas, no sustitutos14.
La vitamina E (tocoferoles y tocotrienoles) protege las membranas celulares contra la peroxidación lipídica. La vitamina C protege los compartimentos acuosos y regenera la vitamina E oxidada. Los carotenoides (betacaroteno, licopeno, luteína, zeaxantina) protegen las membranas y la piel contra los UV. El licopeno del tomate es el carotenoide más potente gracias a su larga cadena de dobles enlaces conjugados. Los polifenoles (flavonoides, resveratrol, curcumina, catequinas del té verde) actúan como antioxidantes pero también como moduladores de la expresión génica a través de las vías NRF2 y NF-κB.
El principio fundamental: « diferentes antioxidantes para diferentes compartimentos celulares ». La vitamina E protege las membranas lipídicas. El glutatión y el selenio protegen el citoplasma. La SOD manganeso protege la matriz mitocondrial. El ácido alfa-lipoico cruza todos los compartimentos. Tomar un único antioxidante esperando proteger toda la célula es como poner un solo guardia frente a un castillo que tiene cien puertas.
Los micronutrientes mitocondriales: la lista completa
Aquí está la lista completa de los micronutrientes necesarios para el funcionamiento mitocondrial óptimo15:
- Vitaminas B1 (tiamina), B2 (riboflavina), B3 (niacina), B5 (ácido pantoténico): cofactores de las vías de producción de ATP
- Hierro y cobre: cofactores de los complejos de la cadena respiratoria
- Zinc y manganeso: cofactores de la SOD
- Selenio: cofactor de la GPx
- Ácido alfa-lipoico: antioxidante mitocondrial y cofactor de la piruvato descarboxilasa
- Coenzima Q10: transportador de electrones entre los complejos I y III
- Glutatión reducido: maestro antioxidante intracelular
- L-carnitina: transportador de ácidos grasos a través de la membrana mitocondrial
- Omega-3 (DHA): componente esencial de la membrana mitocondrial interna (fluidez)
- Vitamina E y vitamina C: antioxidantes exógenos complementarios
- Vitamina A: regulación de la biogénesis mitocondrial
- L-glutamina: sustrato energético de los enterocitos y de los linfocitos
La historia de los pájaros migradores ilustra magníficamente el papel de los omega-3. El correlimos semipalmado (Calidris pusilla) duplica su masa corporal en dos semanas alimentándose de camarones ricos en EPA y DHA antes de un vuelo directo sobre el Atlántico. Los omega-3 se incorporan en las membranas de sus músculos locomotores, aumentan la fluidez membranaria, estimulan la biogénesis mitocondrial y mejoran la capacidad aeróbica16. No es solo energía almacenada, es una señal metabólica que prepara los músculos para la resistencia.
El círculo vicioso mitocondrial
Existe un círculo vicioso que está en el corazón de la medicina mitocondrial. Las mutaciones del ADN mitocondrial (10 veces más frágil que el ADN nuclear pues no está protegido por histonas y dotado de mecanismos de reparación arcaicos) alteran las proteínas de los complejos respiratorios. Los complejos defectuosos dejan caer más electrones. Más electrones que caen significa más radicales libres. Más radicales libres dañan más el ADN mitocondrial. Y el ciclo se acelera con la edad17.
Este círculo vicioso está implicado en las enfermedades del hígado, la diabetes, la obesidad, las enfermedades cardiovasculares, el cáncer, el Alzheimer, el autismo, la fatiga crónica y el envejecimiento acelerado. La teoría mitocondrial del envejecimiento, desarrollada por Harman ya en 1972 y confirmada por Lenaz (1999), considera las mutaciones somáticas del ADN mitocondrial inducidas por los radicales libres como la causa primaria de la declinación energética relacionada con la edad18.
Un ambiente nutricional mitocondrial óptimo es un requisito previo para preservar la salud y garantizar un envejecimiento armonioso. La salud mitocondrial no es un tema de nicho para biólogos. Es el fundamento de toda la salud.
Protocolo naturista anti-estrés oxidativo
Aquí está el protocolo en tres ejes que utilizo en consulta después de un balance oxidativo completo.
Eje 1: Restaurar las defensas endógenas. Esta es la prioridad absoluta. Selenio 100 a 200 µg/día (selenometionina). Zinc bisglicina 15 a 25 mg/día (cofactor SOD1). Manganeso 2 a 5 mg/día (cofactor SOD2). NAC 600 a 1200 mg/día (precursor del glutatión). Ácido alfa-lipoico 300 a 600 mg/día (regenerador de todos los antioxidantes). CoQ10 ubiquinol 100 a 200 mg/día (especialmente si estatinas, fatiga, cardiopatía). El magnesio es un cofactor indirecto (MgATP, SOD).
Eje 2: Aportar los antioxidantes exógenos complementarios. Vitamina C 500 a 1000 mg/día (fraccionada en 2 tomas). Vitamina E natural (mezcla de tocoferoles, no alfa-tocoferol aislado) 200 a 400 UI/día. Carotenoides mixtos (licopeno, luteína, betacaroteno natural) a través de la alimentación colorida. Polifenoles: curcumina (200 a 500 mg/día), resveratrol, EGCG del té verde, quercetina.
Eje 3: Reducir las fuentes de radicales libres. Limitar la exposición a xenobióticos. Gestionar el estrés crónico (fuente de inflamación y de ROS). Practicar una actividad física moderada (el deporte a intensidad moderada aumenta las defensas endógenas; el sobreentrenamiento las agota). Tratar la inflamación crónica de bajo grado. Corregir las carencias en hierro (anemia) y vigilar el exceso de hierro (sobrecarga). Privilegiar la cocción suave (la cocción a alta temperatura genera productos de Maillard pro-oxidantes).
Cuándo consultar y límites del enfoque
Thomas, después de cuatro meses de corrección dirigida basada en su balance oxidativo, vio normalizarse sus marcadores. Su selenio pasó de 65 a 112 µg/L. Su GPx se normalizó. Su glutatión reducido remontó. Y lo más importante, su fatiga desapareció, sus dolores articulares se disolvieron y su vitalidad regresó. Sigue tomando antioxidantes, pero no los del supermercado. Toma selenio, NAC, ácido alfa-lipoico y CoQ10. Sus fundaciones están restauradas. La fachada siguió.
El balance oxidativo es una herramienta poderosa pero requiere un laboratorio especializado e interpretación por un profesional formado. Los marcadores deben interpretarse juntos, no aisladamente. Un exceso de SOD con una GPx baja indica que la primera línea de defensa funciona pero que la segunda está deficiente (déficit en selenio o en glutatión). Un exceso de TBARS con defensas normales indica una fuente exógena de radicales libres (tabaco, contaminación, medicamentos). Cada perfil es único y la corrección debe ser individualizada.
El límite de este enfoque es que el estrés oxidativo nunca está aislado. Está vinculado a la inflamación, a la insulinorresistencia, a la disbacteriosis, a la carga tóxica y al estrés crónico. El balance completo de los 7 pilares de la medicina nutricional a menudo es necesario para entender el conjunto del cuadro. Pero si debiera quedarte con una sola cosa de este artículo, recuerda esto: tus células necesitan selenio, zinc, glutatión y CoQ10 para defenderse. No vitamina C en comprimido efervescente.
Para ir más lejos
- Balance oxidativa: el test del Dr Brack para medir tu estrés oxidativo
- Balance oxidativa de Marchesseau: radicales libres, envejecimiento y defensas antioxidantes
- Cáncer y alimentación: lo que la micronutrición cambia en la ecuación
- Colesterol y enfermedades cardiovasculares: los verdaderos culpables que tu cardiólogo no busca
Fuentes
Footnotes
-
Castronovo V. DU MAPS 2020, curso #13 “Metabolismo Energético: Estrés Oxidativo”. Diapositiva: « Sistemas antioxidantes seguros y eficaces. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « Un individuo quema aproximadamente 50 kilos de ATP al día. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « 3 cuatrillones de mitocondrias por individuo. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositivas: « NAD: vitamina B3; FAD: vitamina B2. Cadena de transporte de electrones. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « 10 % de los electrones altamente energéticos caen de la cadena de transporte. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositivas: « Radicales libres de origen endógeno: mitocondria, inflamación, detoxicación. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « Fluidez membranaria y DHA: dopaje natural en pájaros migradores. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositivas: « SOD (Cu,Zn / Mn) → GPx (Se, GSH) → Catalasa. Reacción de Fenton. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « Sistema de Glutatión Peroxidasa. Todo déficit en selenio provoca acumulación de H2O2. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « NO tenemos sistema enzimático para destruir el radical OH•. Reacción de Fenton. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « 30 % de los franceses tienen déficit de selenio. » ↩
-
Brooks JD et al. Plasma selenium level before diagnosis and the risk of prostate cancer development. J Urol. 2001;166(6):2034-8. Citado en diapositiva Castronovo. ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositivas: « Ácido alfa-lipoico: The Universal Antioxidant. Regenera vitamina C, E, glutatión, tiorredoxina, ubiquinona. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « Diferentes antioxidantes para diferentes compartimentos celulares. » ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « Micronutrientes mitocondriales: lista completa. » ↩
-
Weber JM. The physiology of long-distance migration: extending the limits of endurance metabolism. J Exp Biol. 2009;212:593-597. Citado en diapositiva Castronovo. ↩
-
Castronovo V. DU MAPS 2020, curso #13. Diapositiva: « ADN mitocondrial 10 veces más frágil. Círculo vicioso mutaciones → ROS → mutaciones. » ↩
-
Lenaz G et al. Mitochondria, oxidative stress, and antioxidant defences. Acta Biochim Pol. 1999;46(1):1-21. Citado en diapositiva Castronovo. ↩

Laisser un commentaire
Sois le premier à commenter cet article.