Otto donne un rapporto che dovrebbe far riflettere ogni endocrinologo, ogni ginecologo, ogni medico che prescrive Levotiroxina senza mai chiedersi perché sono le donne a riempire le sale d’attesa. Non gli uomini. Le donne. Otto volte su dieci.
In cinque anni di consultazioni tiroidee, ho ricevuto centinaia di donne con lo stesso profilo. TSH « nella norma », T3 libera sotto il pavimento funzionale, affaticamento cronico, aumento di peso inspiegato, sensibilità al freddo, offuscamento mentale. E ogni volta, la stessa domanda senza risposta: perché io? Perché adesso? Perché dalla pillola, dalla gravidanza, dalla menopausa?
La risposta sta in una parola che nessuno pronuncia in consultazione: gli estrogeni. Non gli estrogeni come « ormoni femminili » nel senso vago del termine. Gli estrogeni come perturbatori diretti del metabolismo tiroideo, attraverso un meccanismo biochimico preciso, documentato, misurabile, e tuttavia sistematicamente ignorato.
« Quando uno dei messaggeri manca all’appello, tutto il sistema compensa, spesso male. » Dr Thierry Hertoghe
Se vuoi prima comprendere le basi del funzionamento tiroideo e i suoi sette cofattori essenziali, inizia dal mio articolo sulla tiroide e la micronutrizione. Qui parleremo del legame profondo tra i tuoi ormoni femminili e la tua tiroide, questo nodo che la medicina non scioglie mai perché guarda ogni filo separatamente.
Il meccanismo che nessuno ti ha spiegato
Bisogna iniziare da un attore invisibile che non troverai su nessuna ricetta: la TBG, globulina legante la tiroxina. È la proteina di trasporto degli ormoni tiroidei nel sangue. La T4 e la T3 non circolano liberamente. Sono legate a questa proteina, come passeggeri su un autobus. E solo gli ormoni che scendono dall’autobus, quelli che chiamiamo « liberi » (T4 libera, T3 libera), possono entrare nelle cellule e agire.
Il problema è che gli estrogeni aumentano la produzione di TBG da parte del fegato. Più estrogeni ci sono nel sangue, più il fegato produce TBG, e più gli ormoni tiroidei vengono sequestrati sulle loro proteine di trasporto. Rimane meno T3 libera disponibile per le cellule. Il tuo esame del sangue può mostrare una T4 totale normale, una TSH corretta, e tuttavia le tue cellule gridano fame perché la T3 libera è prigioniera. Come ricorda Hertoghe in The Hormone Handbook, gli estrogeni in eccesso aumentano la TBG e riducono gli ormoni tiroidei liberi, creando un quadro di ipotiroidismo funzionale che il dosaggio della TSH da solo non rileva.
Questo meccanismo spiega da solo perché le donne sono otto volte più colpite degli uomini. Non è una debolezza. È una conseguenza biochimica diretta della fisiologia femminile. Ogni volta che gli estrogeni aumentano, la TBG aumenta, e la T3 libera disponibile cala. E ogni periodo della vita di una donna in cui gli estrogeni fluttuano violentemente diventa un periodo a rischio per la tiroide.
Il mio articolo sulla tiroide e il fegato dettaglia questa relazione bidirezionale: il fegato converte il 60% della T4 in T3, ma produce anche la TBG. Quando il fegato è sovraccarico di estrogeni, produce troppa TBG e non converte più abbastanza T3. Doppio svantaggio.
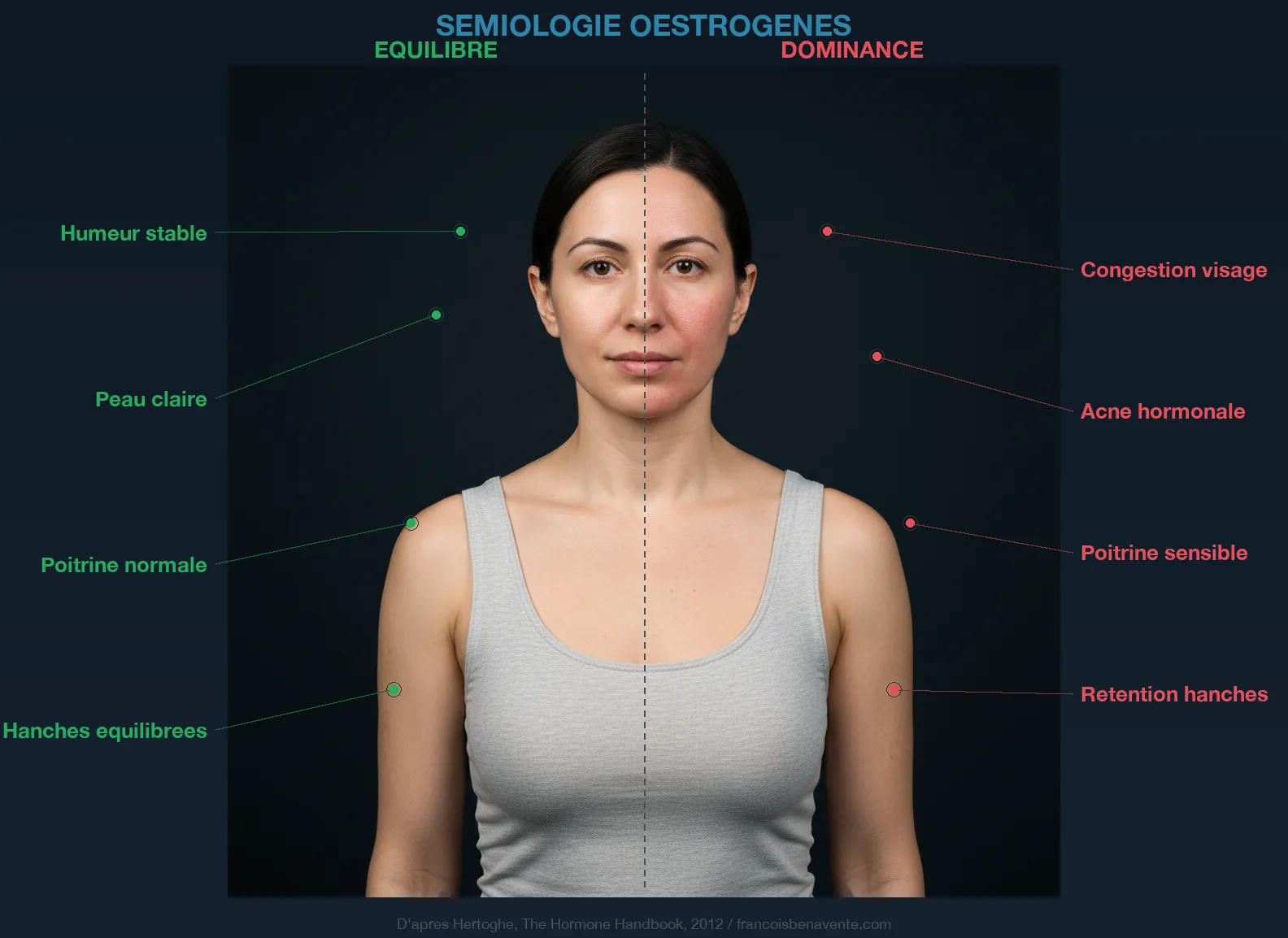
Il problema non viene solo dagli estrogeni in eccesso
Si pensa spesso a « dominanza estrogenica » quando si parla di questo squilibrio. Ma come spiego nell’articolo sui cicli mestruali dolorosi, dominanza non significa eccesso. Si possono avere estrogeni nella fascia bassa della norma ed essere comunque in dominanza se il progesterone è ancora più basso. È il rapporto che conta, non il valore assoluto.
Il progesterone è l’antagonista naturale degli estrogeni. Riduce i recettori degli estrogeni, diminuisce la loro attività, desensibilizza i recettori all’aldosterone (effetto diuretico), e sostiene indirettamente la tiroide mantenendo l’equilibrio ormonale globale. Hertoghe lo conferma: l’estradiolo è dieci volte più potente dell’estrone, e senza un progesterone sufficiente per controbilanciarlo, impone la sua legge a tutto l’organismo. Conseguenze: infertilità, endometriosi, PCOS, fibromi, ritenzione idrica, e ovviamente, blocco tiroideo via TBG.
Perché il progesterone cala? La prima causa è lo stress cronico. Il progesterone condivide un precursore con il cortisolo: la pregnenolone. Quando il corpo è in stress permanente, la pregnenolone viene deviata verso la produzione di cortisolo a scapito del progesterone. È il « furto di pregnenolone » che spiego in dettaglio nell’articolo sullo stress, il cortisolo e le ghiandole surrenali. Poi vengono le carenze di magnesio, litio, zinco, rame e manganese, cofattori indispensabili della sintesi di progesterone. Le diete estreme, che privano il corpo di colesterolo (precursore di tutti gli ormoni steroidei), e le statine, che bloccano la HMG-CoA reduttasi, impoveriscono anche la materia prima. Hertoghe aggiunge un fattore che osservo quotidianamente: quando la tiroide e le surrenali sono stanche, c’è poco o nessun’ovulazione, il che crea uno squilibrio favorendo la formazione di cisti ovariche.
Tutte queste malattie, endometriosi, PCOS, fibromi, tumori estrogeno-dipendenti, condividono un denominatore comune: uno squilibrio estrogeni/progesterone associato a glicemia a digiuno elevata. È un’osservazione clinica costante che Hertoghe e le mie stesse consultazioni confermano.
I quattro periodi a rischio della tua vita
Penso a Lea (nome modificato), 17 anni, portata da sua madre. Affaticamento da un anno, cicli caotici, acne, caduta dei capelli. Il medico curante ha detto « è l’adolescenza ». La TSH era a 3,8 mU/L, « nella norma ». La sua T3 libera non era stata dosata. Quando l’ho richiesta, era a 2,6 pmol/L. Il bassifondi. E nessuno aveva collegato la tempesta estrogenica della pubertà a questa tiroide che si staccava in silenzio.
Quattro momenti della vita femminile concentrano l’essenziale dei triggering tiroidei. Non sono coincidenze. Sono crocevia ormonali dove gli estrogeni si muovono, dove la TBG segue, e dove la tiroide ne soffre.
La pubertà e la pillola costituiscono il primo crocevia. Alla pubertà, gli estrogeni esplodono. La TBG sale. È il momento in cui molte ragazze iniziano a sviluppare sintomi tiroidei diffusi che nessuno identifica: affaticamento, aumento di peso, disturbi di concentrazione, sensibilità al freddo. Lo si attribuisce all’adolescenza. E poi arriva la pillola, spesso prescritta a partire da 15 o 16 anni per cicli dolorosi o acne. Gli estrogeni sintetici contenuti nella pillola aumentano la TBG esattamente come gli estrogeni naturali. Peggio: sovraccaricano il fegato, che ora deve metabolizzare molecole sintetiche in più alle sue funzioni abituali. La conversione da T4 a T3 rallenta. Le riserve di zinco crollano (i lavori di Curtay confermano che il livello di vitamina B6 cala nelle donne in pillola da più di due anni, e lo zinco segue la stessa traiettoria). Il magnesio crolla. E il progesterone naturale viene messo in pausa poiché la pillola sopprime l’ovulazione.
Mi ritorna in mente Sarah (nome modificato), 26 anni, venuta da me dopo otto anni di pillola. L’aveva smessa per un progetto di bambino, e da allora, tutto crollava. Cicli assenti, affaticamento schiacciante, dieci chili in sei mesi. Il suo ginecologo le aveva proposto di riprendere la pillola « nel frattempo che si calmi ». Nessuno aveva dosato la sua T3 libera, il suo zinco, il suo magnesio, la sua vitamina D. Nessuno aveva guardato il suo fegato. Il suo corpo gridava che otto anni di estrogeni sintetici avevano svuotato le riserve e bloccato la conversione tiroidea. L’articolo su l’ipotiroidismo come sintomo spiega perché questo vagabondaggio diagnostico è così frequente.
La gravidanza e il post-partum formano il secondo crocevia, e probabilmente il più violento. Durante la gravidanza, gli estrogeni sono moltiplicati per trenta. È necessario per lo sviluppo della placenta, la vascolarizzazione uterina, la crescita del bambino. Ma la conseguenza tiroidea è massiccia: la TBG esplode, e la T3 libera disponibile per la madre crolla drasticamente. Il corpo del bambino ha bisogno di T3 per costruire il cervello (un terzo di EPA) e le guaine di mielina dei suoi neuroni (un terzo di DHA). E come precisano i lavori di Curtay e Hertoghe, la T4 non attraversa la placenta, solo la T3 conta. Qualsiasi insufficienza di T3 materna si ripercuote direttamente sullo sviluppo neurologico del feto.
L’American Thyroid Association raccomanda una TSH inferiore a 2,5 mU/L per la concezione. Questa soglia è molto più ristretta delle normali gamme di laboratorio, e tuttavia raramente viene verificata. Una donna su cinque che ha avuto un aborto spontaneo presenta un problema tiroideo. E le carenze si accumulano: l’anemia moltiplica per 2,5 a 3 il rischio di complicazioni ostetriche. Curtay riferisce che l’80% delle donne è carente di magnesio (studio del Val-de-Marne), e il 100% delle donne in età fertile non copre i propri fabbisogni di zinco attraverso l’alimentazione. La gravidanza attinge da riserve già vuote.
Dopo il parto, il calo degli ormoni placentari crea un vuoto ormonale brutale. La tiroidite del post-partum colpisce il 5-10% delle donne. Spesso passa inosservata perché la stanchezza, i disturbi dell’umore e l’aumento di peso sono attribuiti alla mancanza di sonno e all’« adattamento alla vita di mamma ». È una diagnosi che dovrebbe essere sistematicamente ricercata nei sei mesi successivi a un parto.
La perimenopausa, tra i 40 e i 50 anni circa, è il terzo crocevia. È il periodo più insidioso perché gli ormoni non diminuiscono in modo lineare. Oscillano. Un ciclo, gli estrogeni sono al massimo. Quello seguente, sono al minimo. Il progesterone, invece, cala in modo più regolare poiché l’ovulazione diventa intermittente. Risultato: mesi di intensa dominanza estrogenica si alternano a mesi di carenza globale. La tiroide subisce queste montagne russe senza rete di sicurezza. È il periodo in cui vediamo comparire i Basedow tardivi, le ipotiroidie « nuove » in donne che non avevano mai avuto un problema. L’articolo su Hashimoto spiega come il meccanismo autoimmune può attivarsi quando il terreno è fragilizzato da questa instabilità ormonale.
La menopausa chiude il ciclo. Gli estrogeni calano definitivamente, ma la tiroide non si recupera. Anni di dominanza estrogenica hanno esaurito il fegato, svuotato le riserve di cofattori, e talvolta innescato un processo autoimmune irreversibile. Inoltre, il calo degli estrogeni è accompagnato da una perdita ossea accelerata, da un aumentato rischio cardiovascolare, e da un rallentamento metabolico che aggrava i sintomi tiroidei. È spesso in questo momento che interviene la prescrizione di Levotiroxina, senza che nessuno cerchi di comprendere i decenni di squilibrio che hanno portato qui.
I buoni e i cattivi estrogeni
Non tutti gli estrogeni si equivalgono, ed è una sfumatura fondamentale. Il fegato metabolizza gli estrogeni attraverso gli enzimi del citocromo P450, e a seconda della via intrapresa, il risultato è radicalmente diverso.
Gli enzimi CYP1A1 e CYP3A4 idrossilano gli estrogeni in posizione 2. I metaboliti 2-OH hanno un’attività estrogenica debole. Sono protettivi, antiproliferativi, associati a un minor rischio di cancro. È la via che vuoi favorire.
L’enzima CYP1B1 idrossila in posizione 4. I metaboliti 4-OH sono potenzialmente genotossici, capaci di formare addotti al DNA.
E poi c’è la via 16-alfa-OH. I metaboliti 16-alfa-OH conservano un’attività estrogenica elevata, sono pro-infiammatori, e stimolano la proliferazione cellulare. E qui c’è il collegamento che nessuno fa: gli estrogeni 16-alfa aumentano l’epcidina, questo ormone epatico che blocca l’assorbimento intestinale del ferro e lo sequestra nei macrofagi. È il ponte tra l’eccesso di estrogeni e l’anemia che molte donne trascinano senza spiegazione. Meno ferro disponibile significa anche meno perossidasi tiroidea funzionale, e quindi meno produzione di ormoni tiroidei.
Esiste un’ipotesi clinica affascinante che osservo in consultazione: l’eccesso di metaboliti 16-alfa-OH potrebbe spiegare il rapporto di dieci donne per un uomo nelle tiroiditi autoimmuni. Sono questi metaboliti pro-infiammatori che mantengono la cascata immunitaria descritta da Seignalet, questa risposta xeno-immune che finisce per attaccare la tiroide. Gli uomini, con livelli di estrogeni da dieci a venti volte inferiori, sono naturalmente protetti da questo meccanismo.
Per orientare verso la via protettiva 2-OH, il fegato ha bisogno di crucifere (broccoli, cavolo riccio, rucola, ravanelli, germogli di broccoli ricchi di sulforafano e indolo-3-carbinolo), vitamina B6, magnesio, e di una metilazione efficace (B9 sotto forma di 5-MTHF, B12 metilcobalamina, betaina). Il DIM (diindolilmetano) è il metabolita attivo dell’indolo-3-carbinolo. È uno dei integratori che prescrivo quotidianamente in consultazione alle donne con un profilo estrogenico sfavorevole. Curtay insiste su un punto cruciale: la forma di B9 conta. Il 5-MTHF è la forma attiva, non l’acido folico sintetico che si trova nella maggior parte degli integratori prenatali.
Il fegato, crocevia obbligato
L’hai capito, il fegato è al centro di tutto. Converte il 60% della T4 in T3 attiva. Produce la TBG. Metabolizza gli estrogeni attraverso i citocromi P450. Produce la bile che elimina i metaboliti estrogenici coniugati. E sintetizza il colesterolo, precursore di tutti gli ormoni steroidei (incluso il progesterone).
Quando il fegato è sovraccarico, tutto crolla allo stesso tempo. La conversione da T4 a T3 rallenta, come dettagliato nel mio articolo sulla tiroide e il fegato. La TBG aumenta perché il fegato continua a produrla sotto l’effetto degli estrogeni che non riesce più a eliminare. Gli estrogeni non metabolizzati ritornano in circolazione (ciclo entero-epatico). La produzione di bile diminuisce, rallentando il transito e favorendo il riassorbimento degli estrogeni dall’estroboloma intestinale, questi batteri che producono la beta-glucuronidasi.
È un circolo vizioso che osservo quotidianamente. L’ipotiroidismo rallenta il metabolismo epatico. Il fegato congestionato non metabolizza più gli estrogeni. Gli estrogeni aumentano la TBG. La T3 libera cala. L’ipotiroidismo peggiora. Il fegato rallenta ancora. E così via. Il Dr Mouton parla di « fegato grasso tiroideo » per descrivere la steatosi che accompagna così spesso l’ipotiroidismo cronico.
Gli xenoestrogeni aggiungono un ulteriore strato. Carne non biologica, latte convenzionale, pesticidi, plastiche, cosmetici convenzionali, PFAS delle padelle antiaderenti, acqua del rubinetto contaminata. Queste molecole imitano l’azione degli estrogeni, saturano i recettori, e sovraccaricano un fegato già sopraffatto. L’EFSA (Autorità europea per la sicurezza alimentare) ha identificato 101 pesticidi su 287 valutati che colpiscono direttamente la tiroide. È un terzo.
La disfunzione intestinale che amplifica tutto
L’intestino gioca un ruolo che sistematicamente sottovalutiamo. L’estroboloma, questo insieme di batteri intestinali capaci di metabolizzare gli estrogeni, può diventare il tuo peggior nemico. In caso di disbiosi, alcuni batteri surproducono la beta-glucuronidasi, un enzima che deconiuga gli estrogeni che il fegato aveva preparato per l’eliminazione. Invece di essere evacuati nelle feci, gli estrogeni vengono riassorbiti e rispediti in circolazione. La dominanza estrogenica peggiora senza che tu abbia consumato nemmeno un singolo perturbatore endocrino.
La candidosi intestinale complica il quadro. Il Candida albicans fragilizza le giunzioni strette dell’epitelio, creando una permeabilità intestinale che lascia passare macromolecole pro-infiammatorie. E nel contesto di Hashimoto, questa permeabilità è il punto di partenza della cascata autoimmune descritta da Seignalet: i peptidi antigenici attraversano la barriera, si accumulano nei tireociti, e il sistema immunitario attacca la tiroide. Il Candida cattura anche il magnesio attraverso la produzione di tricarbossilato, impoverendo ulteriormente un organismo già carente.
Il transito è fondamentale. La stitichezza è il nemico di ogni donna in dominanza estrogenica. Senza un transito quotidiano, gli estrogeni coniugati dal fegato ed escreti nella bile ristagnano e vengono riassorbiti. L’ipotiroidismo stesso rallenta la peristalsi. È un ulteriore circolo vizioso.
Il piatto prima della compressa
Marchesseau lo ripeteva: « Non uccidete le zanzare, prosciugate la palude. » Prima di qualsiasi integrazione, l’alimentazione. E nel contesto tiroide-ormoni femminili, il piatto agisce simultaneamente su entrambi i fronti.
Le crucifere sono la prima leva. Broccoli, cavolo riccio, cavolfiore, rucola, ravanelli, navone. I germogli di broccoli sono i più concentrati in sulforafano. Il sulforafano attiva gli enzimi di fase II del fegato (glucuronidazione, solfonazione) e l’indolo-3-carbinolo orienta gli estrogeni verso la via protettiva 2-OH. Li prescrivo quotidianamente. La decozione zenzero-rosmarino del mattino cumula un effetto epatoprotettivo, colagogo e antinfiammatorio. Lo zenzero inibisce la COX-2 con un’efficacia paragonabile all’ibuprofene negli studi clinici sulla dismenorrea, senza gli effetti collaterali gastrici.
Ridurre gli omega-6 eccessivi (olio di girasole, prodotti trasformati, fritture) e aumentare gli omega-3 (piccoli pesci grassi tre volte a settimana, olio di lino o camelina come condimento). Il rapporto ideale omega-6/omega-3 è di 1 a 3. L’alimentazione occidentale è spesso a 20 a 1. Questo squilibrio alimenta l’infiammazione cronica che aggrava sia la dominanza estrogenica che l’ipotiroidismo.
Le proteine di qualità, soprattutto al mattino: uova biologiche, piccoli pesci grassi, noci. Target: 1,2 g per kg di peso corporeo al giorno. Gli amminoacidi sono i precursori dei neurotrasmettitori e degli ormoni. La tirosina, precursore diretto degli ormoni tiroidei, è fornita dalle proteine animali.
Le esclusioni prioritarie: zucchero raffinato (resistenza all’insulina, candidosi, infiammazione), alcol (sovraccarico epatico diretto), soia non fermentata in eccesso (fitoestrogeni nelle donne in dominanza), latticini convenzionali (xenoestrogeni, caseina pro-infiammatoria), glutine se permeabilità intestinale sospetta. L’articolo sulle basi della naturopatia dettaglia la riforma alimentare globale.
I cofattori che sbloccano la situazione
Penso a Natalie (nome modificato), 43 anni, in perimenopausa. Affaticamento intenso da due anni, aumento di sette chili, pelle secca, cicli diventati anarchici. TSH a 3,4 mU/L, « nella norma ». T3 libera a 2,9 pmol/L. Estradiolo fluttuante. Progesterone al minimo. Zinco plasmatico a 0,55 mg/L (norma bassa). Magnesio eritrocitario basso. Vitamina D a 19 ng/mL. Ferritina a 25 ng/mL. A nessuno era venuto in mente di prescriverle questo esame. Il suo endocrinologo controllava la TSH, il suo ginecologo proponeva un trattamento ormonale sostitutivo. Nessuno dei due guardava i cofattori.
Lo zinco innanzitutto. Cofattore della conversione da T4 a T3, cofattore della delta-6-desaturasi (che converte gli omega-3 in prostaglandine antinfiammatorie), modulatore immunitario. Secondo il Dr Claeys, più del 90% dei pazienti tiroidei è carente di zinco. E Curtay conferma che il 100% delle donne in età fertile non copre i propri fabbisogni attraverso l’alimentazione. Zinco bisglicinato, 15-25 mg al giorno, lontano dai pasti ricchi di ferro e calcio.
Il magnesio poi. Anti-stress, miorilassante, cofattore di più di 300 reazioni enzimatiche. L’80% delle donne è carente secondo lo studio del Val-de-Marne. Il magnesio sostiene le surrenali (meno furto di pregnenolone), rilassa il muscolo uterino, e partecipa alla conversione da T4 a T3. Magnesio bisglicinato o malato, 300-400 mg al giorno, in due dosi.
La vitamina B6 sotto forma di P5P (piridossale-5-fosfato, la forma attiva). Cofattore della delta-6-desaturasi, cofattore della disintossicazione epatica degli estrogeni in fase II, cofattore della sintesi di progesterone e di serotonina. La pillola consuma B6, gli estrogeni in eccesso consumano B6, e senza B6, né la conversione degli omega-3 né la disintossicazione degli estrogeni avvengono correttamente. P5P, 50 mg al giorno.
Il selenio: cofattore della 5’-deiodinasi (conversione da T4 a T3), cofattore della glutatione perossidasi (antiossidante tiroideo maggiore). Selenometionina, 100-200 microgrammi al giorno. Indispensabile prima di qualsiasi integrazione di iodio, soprattutto in caso di Hashimoto.
Gli omega-3 EPA e DHA: precursori delle prostaglandine antinfiammatorie PGE3 e delle risolvine. L’EPA è il precursore diretto dei PGE3 che rilassano il muscolo uterino e riducono l’infiammazione. Olio di pesce o microalghe, 2-3 g al giorno.
La vitamina D3: immunomodulatrice, antinfiammatoria. Lo studio ENNS mostra che più dell’80% della popolazione francese è in insufficienza. Obiettivo ematico: 60 ng/mL. Vitamina D3, 2.000-4.000 UI al giorno, con vitamina K2-MK7.
Il ferro, ma solo dopo dosaggio della ferritina. Obiettivo: 50-90 ng/mL. Il ferro libero è pro-ossidante (reazione di Fenton). Curtay mette in guardia: ferro più vitamina C in integratore genera radicali idrossile. Preferire l’associazione ferro, magnesio e polifenoli. Non integrare mai alla cieca.
Infine, la B9 sotto forma di 5-MTHF (e mai acido folico sintetico) per sostenere la metilazione epatica e la disintossicazione degli estrogeni. L’omocisteina target è minore o uguale a 7 mg/L. Al di sopra, la metilazione è insufficiente, e gli estrogeni ristagnano.
Per l


Laisser un commentaire
Sois le premier à commenter cet article.