Ocho mujeres por cada dos hombres. Este es el ratio que debería hacer reflexionar a cada endocrinólogo, cada ginecólogo, cada médico que prescribe Levothyrox sin jamás preguntarse por qué son las mujeres quienes llenan las salas de espera. No los hombres. Las mujeres. Ocho de cada diez.
En cinco años de consultas tiroideas, he recibido a cientos de mujeres con el mismo perfil. TSH «dentro de los rangos normales», T3 libre por debajo del piso funcional, fatiga crónica, aumento de peso inexplicado, sensibilidad al frío, confusión mental. Y cada vez, la misma pregunta sin respuesta: ¿por qué yo? ¿Por qué ahora? ¿Por qué desde la píldora, desde el embarazo, desde la menopausia?
La respuesta se resume en una palabra que nadie pronuncia en consulta: los estrógenos. No los estrógenos como «hormonas femeninas» en el sentido vago del término. Los estrógenos como perturbadores directos del metabolismo tiroideo, a través de un mecanismo bioquímico preciso, documentado, medible, y sin embargo sistemáticamente ignorado.
«Cuando uno de los mensajeros falta, todo el sistema compensa, a menudo mal.» Dr Thierry Hertoghe
Si primero quieres comprender los fundamentos del funcionamiento tiroideo y sus siete cofactores esenciales, comienza con mi artículo sobre la tiroides y la micronutrición. Aquí, hablaremos del vínculo profundo entre tus hormonas femeninas y tu tiroides, este nudo que la medicina nunca desata porque observa cada hilo por separado.
El mecanismo que nadie te ha explicado
Hay que empezar por un actor invisible que no encontrarás en ninguna receta: la TBG, globulina fijadora de tiroxina. Es la proteína de transporte de las hormonas tiroideas en la sangre. La T4 y la T3 no circulan libremente. Están unidas a esta proteína, como pasajeros en un autobús. Y solo las hormonas que bajan del autobús, las que llamamos «libres» (T4 libre, T3 libre), pueden entrar en las células y actuar.
El problema es que los estrógenos aumentan la producción de TBG por el hígado. Cuanto más estrógeno hay en la sangre, más TBG fabrica el hígado, y más hormonas tiroideas quedan atrapadas en sus proteínas de transporte. Queda menos T3 libre disponible para las células. Tu análisis de sangre puede mostrar una T4 total normal, una TSH correcta, y sin embargo tus células gritan por hambre porque la T3 libre está cautiva. Como recuerda Hertoghe en The Hormone Handbook, los estrógenos en exceso aumentan la TBG y reducen las hormonas tiroideas libres, creando un cuadro de hipotiroidismo funcional que el solo dosaje de TSH no detecta.
Este mecanismo por sí solo explica por qué las mujeres se ven afectadas ocho veces más que los hombres. No es una debilidad. Es una consecuencia bioquímica directa de la fisiología femenina. Cada vez que los estrógenos suben, la TBG sube, y la T3 libre disponible cae. Y cada período de la vida de una mujer en el que los estrógenos fluctúan violentamente se convierte en un período de riesgo para la tiroides.
Mi artículo sobre la tiroides y el hígado detalla esta relación bidireccional: el hígado convierte el 60% de la T4 en T3, pero también fabrica la TBG. Cuando el hígado está sobrecargado por los estrógenos, produce demasiada TBG y no convierte suficiente T3. Doble castigo.
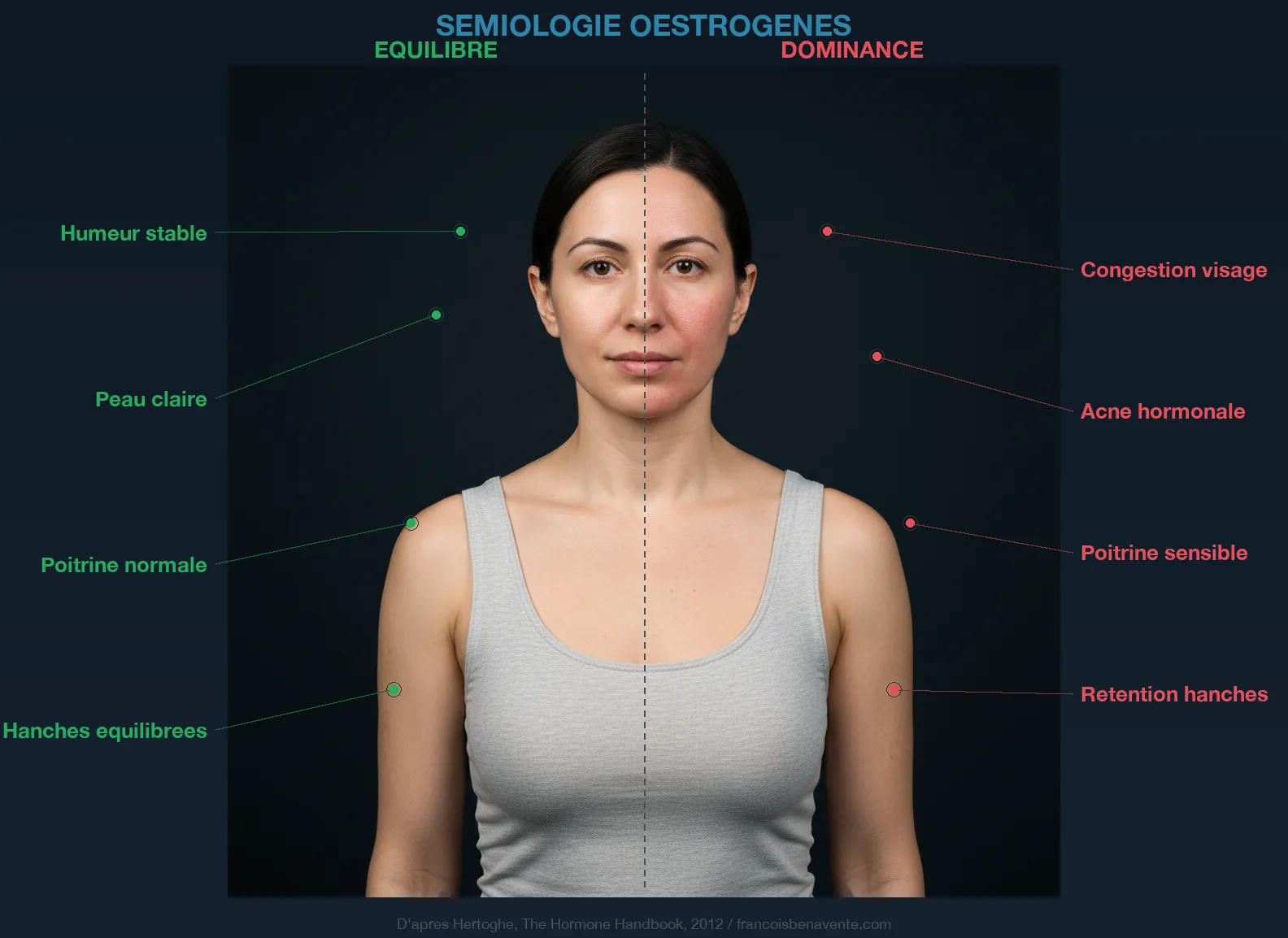
El problema no proviene solo del exceso de estrógenos
A menudo pensamos en «dominancia estrogénica» cuando hablamos de este desequilibrio. Pero como explico en el artículo sobre reglas dolorosas, dominancia no significa exceso. Puedes tener estrógenos dentro de los rangos normales bajos y seguir estando en dominancia si la progesterona es aún más baja. Es la proporción la que importa, no el valor absoluto.
La progesterona es el antagonista natural de los estrógenos. Reduce los receptores de estrógenos, disminuye su actividad, desensibiliza los receptores a la aldosterona (efecto diurético), y apoya indirectamente la tiroides manteniendo el equilibrio hormonal global. Hertoghe lo confirma: el estradiol es diez veces más potente que la estrona, y sin una progesterona suficiente para contrapesarlo, impone su ley a todo el organismo. Consecuencias: infertilidad, endometriosis, SOP, fibromas, retención de agua, y por supuesto, bloqueo tiroideo a través de la TBG.
¿Por qué cae la progesterona? La primera causa es el estrés crónico. La progesterona comparte un precursor con el cortisol: la pregnenolona. Cuando el cuerpo está en estrés permanente, la pregnenolona se desvía hacia la producción de cortisol en detrimento de la progesterona. Este es el «robo de pregnenolona» que explico en detalle en el artículo sobre estrés, cortisol y glándulas suprarrenales. Luego vienen las carencias de magnesio, litio, zinc, cobre y manganeso, cofactores indispensables de la síntesis de progesterona. Las dietas extremas, que privan al cuerpo de colesterol (precursor de todas las hormonas esteroides), y las estatinas, que bloquean la HMG-CoA reductasa, también emporecen la materia prima. Hertoghe añade un factor que observo diariamente: cuando la tiroides y las suprarrenales están fatigadas, hay poco o ningún ciclo ovulatorio, lo que crea un desequilibrio que favorece la formación de quistes ováricos.
Todas estas enfermedades, endometriosis, SOP, fibromas, cánceres estrogéno-dependientes, comparten un denominador común: un desequilibrio estrógenos/progesterona asociado con glucemia en ayunas elevada. Esta es una observación clínica constante que Hertoghe y mis propias consultas confirman.
Los cuatro períodos de riesgo de tu vida
Pienso en Lea (nombre modificado), 17 años, llevada por su madre. Fatiga desde hace un año, reglas caóticas, acné, caída de cabello. El médico de cabecera dijo «es la adolescencia». La TSH estaba en 3,8 mU/L, «dentro de los rangos normales». Su T3 libre no había sido dosificada. Cuando la solicité, estaba en 2,6 pmol/L. El sótano. Y nadie había hecho la conexión entre la tormenta estrogénica de la pubertad y esta tiroides que se desconectaba en silencio.
Cuatro momentos de la vida femenina concentran lo esencial de los desencadenantes tiroideos. No son coincidencias. Son cruces hormonales donde los estrógenos se mueven, donde la TBG los sigue, y donde la tiroides lo paga.
La pubertad y la píldora constituyen el primer cruce. En la pubertad, los estrógenos explotan. La TBG sube. Es el momento en el que muchas adolescentes comienzan a desarrollar síntomas tiroideos difusos que nadie identifica: fatiga, aumento de peso, problemas de concentración, sensibilidad al frío. Se atribuye esto a la adolescencia. Y luego llega la píldora, a menudo prescrita desde los 15 o 16 años para reglas dolorosas o acné. Los estrógenos sintéticos contenidos en la píldora aumentan la TBG exactamente como los estrógenos naturales. Peor aún: sobrecargan el hígado, que ahora debe metabolizar moléculas sintéticas además de sus funciones habituales. La conversión T4 a T3 se ralentiza. Las reservas de zinc se colapsan (los trabajos de Curtay confirman que los niveles de vitamina B6 caen en mujeres bajo píldora por más de dos años, y el zinc sigue la misma trayectoria). El magnesio se desploma. Y la progesterona natural se pone en espera ya que la píldora suprime la ovulación.
Pienso en Sarah (nombre modificado), 26 años, quien vino a verme después de ocho años de píldora. Había dejado para un proyecto de bebé, y desde entonces todo se desmoronaba. Ciclos ausentes, fatiga abrumadora, diez kilos en seis meses. Su ginecólogo le había propuesto reanudar la píldora «mientras se calma». Nadie había dosificado su T3 libre, su zinc, su magnesio, su vitamina D. Nadie había observado su hígado. Su cuerpo gritaba que ocho años de estrógenos sintéticos habían vaciado las reservas y bloqueado la conversión tiroidea. El artículo sobre hipotiroidismo como síntoma explica por qué esta odisea diagnóstica es tan frecuente.
El embarazo y el posparto forman el segundo cruce, y probablemente el más violento. Durante el embarazo, los estrógenos se multiplican por treinta. Es necesario para el desarrollo de la placenta, la vascularización uterina, el crecimiento del bebé. Pero la consecuencia tiroidea es masiva: la TBG explota, y la T3 libre disponible para la madre cae drásticamente. El cuerpo del bebé necesita T3 para construir su cerebro (un tercio de EPA) y las vainas de mielina de sus neuronas (un tercio de DHA). Y como precisan los trabajos de Curtay y Hertoghe, la T4 no atraviesa la placenta, solo cuenta la T3. Toda insuficiencia en T3 materna se repercute directamente en el desarrollo neurológico del feto.
La American Thyroid Association recomienda una TSH inferior a 2,5 mU/L para la concepción. Este umbral es mucho más estricto que las normas de laboratorio habituales, y sin embargo rara vez se verifica. Una de cada cinco mujeres que han tenido un aborto espontáneo presenta un problema tiroideo. Y las carencias se acumulan: la anemia multiplica por 2,5 a 3 el riesgo de complicaciones obstétricas. Curtay reporta que el 80% de las mujeres son deficientes en magnesio (estudio de Val-de-Marne), y el 100% de las mujeres en edad reproductiva no cubren sus necesidades de zinc por la alimentación. El embarazo extrae de reservas que ya están vacías.
Después del parto, la caída de las hormonas placentarias crea un vacío hormonal brutal. La tiroiditis posparto afecta al 5-10% de las mujeres. Pasa a menudo desapercibida porque la fatiga, los trastornos del humor y el aumento de peso se atribuyen a la falta de sueño y a la «adaptación a la vida de mamá». Este es un diagnóstico que debería buscarse sistemáticamente en los seis meses posteriores a un parto.
La perimenopausia, entre los 40 y 50 años aproximadamente, es el tercer cruce. Es el período más traidor porque las hormonas no disminuyen de forma lineal. Oscilan. Un ciclo, los estrógenos están en el techo. El siguiente, están en el piso. La progesterona, por el contrario, cae de forma más regular ya que la ovulación se vuelve intermitente. Resultado: meses de dominancia estrogénica intensa alternan con meses de carencia global. La tiroides sufre estos altibajos sin red de seguridad. Es el período en el que vemos aparecer Hashimoto tardío, hipotiroidismos «nuevos» en mujeres que nunca habían tenido problemas. El artículo sobre Hashimoto explica cómo el mecanismo autoinmune puede desencadenarse cuando el terreno está fragilizado por esta inestabilidad hormonal.
La menopausia cierra el ciclo. Los estrógenos caen definitivamente, pero la tiroides no se recupera por ello. Años de dominancia estrogénica han agotado el hígado, vaciado las reservas de cofactores, y a veces desencadenado un proceso autoinmune irreversible. Además, la caída de estrógenos se acompaña de una pérdida ósea acelerada, un riesgo cardiovascular aumentado, y un ralentización metabólica que agrava los síntomas tiroideos. A menudo es en este momento cuando interviene la prescripción de Levothyrox, sin que nadie busque comprender las décadas de desequilibrio que llevaron allí.
Los buenos y los malos estrógenos
Todos los estrógenos no son iguales, y esta es una matización fundamental. El hígado metaboliza los estrógenos a través de las enzimas del citocromo P450, y según la vía utilizada, el resultado es radicalmente diferente.
Las enzimas CYP1A1 y CYP3A4 hidroxilan los estrógenos en posición 2. Los metabolitos 2-OH tienen una actividad estrogénica débil. Son protectores, antiproliferativos, asociados con menor riesgo de cáncer. Esta es la vía que quieres favorecer.
La enzima CYP1B1 hidroxila en posición 4. Los metabolitos 4-OH son potencialmente genotóxicos, capaces de formar aductos con el ADN.
Y luego está la vía 16-alfa-OH. Los metabolitos 16-alfa-OH conservan una actividad estrogénica elevada, son proinflamatorios, y estimulan la proliferación celular. Y aquí está el vínculo que nadie establece: los estrógenos 16-alfa aumentan la hepcidina, esta hormona hepática que bloquea la absorción intestinal de hierro y lo secuestra en los macrófagos. Este es el puente entre el exceso de estrógenos y la anemia que tantas mujeres arrastran sin explicación. Menos hierro disponible significa también menos tiperoxidasa funcional, y por lo tanto menos producción de hormonas tiroideas.
Existe una hipótesis clínica fascinante que observo en consulta: el exceso de metabolitos 16-alfa-OH podría explicar la proporción de diez mujeres por cada hombre en las tiroiditis autoinmunes. Son estos metabolitos proinflamatorios los que mantienen la cascada inmunitaria descrita por Seignalet, esta respuesta xenoinmune que termina atacando la tiroides. Los hombres, con tasas de estrógenos diez a veinte veces inferiores, están naturalmente protegidos de este mecanismo.
Para orientar hacia la vía protectora 2-OH, el hígado necesita crucíferas (brócoli, col rizada, rúcula, rábano, brotes de brócoli ricos en sulforafano e indol-3-carbinol), vitamina B6, magnesio, y una metilación eficaz (B9 como 5-MTHF, B12 metilcobalamina, betaína). El DIM (diiindolmetano) es el metabolito activo del indol-3-carbinol. Es uno de los suplementos que más prescribo en consulta en mujeres con un perfil estrogénico desfavorable. Curtay insiste en un punto crucial: la forma de B9 importa. El 5-MTHF es la forma activa, no el ácido fólico de síntesis que se encuentra en la mayoría de los suplementos prenatales.
El hígado: cruce obligatorio
Lo has entendido, el hígado está en el centro de todo. Convierte el 60% de la T4 en T3 activa. Fabrica la TBG. Metaboliza los estrógenos a través de los citocromos P450. Produce la bilis que elimina los metabolitos estrogénicos conjugados. Y sintetiza el colesterol, precursor de todas las hormonas esteroides (incluyendo la progesterona).
Cuando el hígado está sobrecargado, todo se desmorona al mismo tiempo. La conversión T4 a T3 se ralentiza, como detalla mi artículo sobre la tiroides y el hígado. La TBG aumenta porque el hígado continúa produciéndola bajo el efecto de los estrógenos que ya no puede eliminar. Los estrógenos no metabolizados vuelven a la circulación (ciclo entero-hepático). La producción de bilis disminuye, ralentizando el tránsito e favoreciendo la reabsorción de estrógenos por el estroboloma intestinal, estas bacterias que producen beta-glucuronidasa.
Este es un círculo vicioso que observo diariamente. La hipotiroides ralentiza el metabolismo hepático. El hígado congestionado no metaboliza más los estrógenos. Los estrógenos aumentan la TBG. La T3 libre cae. La hipotiroides se agrava. El hígado se ralentiza aún más. Y así sucesivamente. El Dr Mouton habla de «hígado graso tiroideo» para describir la esteatosis que acompaña tan a menudo a la hipotiroidismo crónico.
Los xenoestrógenos añaden otra capa. Carne no orgánica, leche convencional, pesticidas, plásticos, cosméticos convencionales, PFAS de las sartenes antiadherentes, agua del grifo contaminada. Estas moléculas imitan la acción de los estrógenos, saturan los receptores, y sobrecargan un hígado ya desbordado. La EFSA (Autoridad Europea de Seguridad Alimentaria) ha identificado 101 pesticidas de 287 evaluados que afectan directamente la tiroides. Es un tercio.
El disfuncionamiento intestinal que amplifica todo
El intestino juega un rol que subestimamos sistemáticamente. El estroboloma, este conjunto de bacterias intestinales capaces de metabolizar los estrógenos, puede convertirse en tu peor enemigo. En caso de disbiosis, ciertas bacterias sobreproduren beta-glucuronidasa, una enzima que desconjuga los estrógenos que el hígado había preparado para la eliminación. En lugar de ser evacuados en las heces, los estrógenos son reabsorbidos y devueltos a la circulación. La dominancia estrogénica se agrava sin que hayas consumido ni un solo perturbador endocrino.
La candidiasis intestinal complica el cuadro. El Candida albicans fragiliza las uniones estrechas del epitelio, creando una permeabilidad intestinal que deja pasar macromoléculas proinflamatorias. Y en el contexto de Hashimoto, esta permeabilidad es el punto de partida de la cascada autoinmune descrita por Seignalet: los péptidos antigénicos atraviesan la barrera, se acumulan en los tirocitos, y el sistema inmunitario ataca la tiroides. El Candida también captura el magnesio a través de la producción de tricarbalilato, emporeciendo aún más un organismo ya deficiente.
El tránsito es fundamental. El estreñimiento es el enemigo de toda mujer en dominancia estrogénica. Sin un tránsito diario, los estrógenos conjugados por el hígado y excretados en la bilis se estancan y son reabsorbidos. La hipotiroidismo en sí misma ralentiza el peristaltismo. Este es otro círculo vicioso adicional.
La comida antes de la píldora
Marchesseau lo repetía: «No mates los mosquitos, seca la ciénaga.» Antes de cualquier suplementación, la alimentación. Y en el contexto tiroides-hormonas femeninas, la comida actúa simultáneamente en ambos frentes.
Las crucíferas son el primer apalancamiento. Brócoli, col rizada, coliflor, rúcula, rábano, nabo. Los brotes de brócoli son los más concentrados en sulforafano. El sulforafano activa las enzimas de fase II del hígado (glucuronidación, sulfonación) y el indol-3-carbinol orienta los estrógenos hacia la vía protectora 2-OH. Los prescribo diariamente. La decocción jengibre-romero de la mañana combina un efecto hepatoprotector, colagogo y antiinflamatorio. El jengibre inhibe las COX-2 con una eficacia comparable al ibuprofeno en los estudios clínicos sobre dismenorrea, sin los efectos secundarios gástricos.
Reducir los omega-6 excesivos (aceite de girasol, productos procesados, frituras) e incrementar los omega-3 (peces grasos pequeños tres veces a la semana, aceite de lino o camelia como aderezo). La proporción ideal omega-6/omega-3 es de 1 por 3. La alimentación occidental suele estar a 20 por 1. Este desequilibrio alimenta la inflamación crónica que agrava tanto la dominancia estrogénica como la hipotiroidismo.
Las proteínas de calidad, especialmente por la mañana: huevos ecológicos, peces grasos pequeños, frutos secos. Objetivo: 1,2 g por kg de peso corporal por día. Los aminoácidos son los precursores de los neurotransmisores y las hormonas. La tirosina, precursor directo de las hormonas tiroideas, se aporta a través de las proteínas animales.
Las exclusiones prioritarias: azúcar refinado (resistencia a la insulina, candidiasis, inflamación), alcohol (sobrecarga hepática directa), soja no fermentada en exceso (fitoestrógenos en mujeres en dominancia), productos lácteos convencionales (xenoestrógenos, caseína proinflamatoria), gluten si permeabilidad intestinal sospechada. El artículo sobre los fundamentos de la naturopatía detalla la reforma alimentaria global.
Los cofactores que desbloquean la situación
Pienso en Natalie (nombre modificado), 43 años, en perimenopausia. Fatiga intensa desde hace dos años, aumento de siete kilos, piel seca, reglas vueltas caóticas. TSH a 3,4 mU/L, «dentro de los rangos normales». T3 libre a 2,9 pmol/L. Estradiol fluctuante. Progesterona en el piso. Zinc plasmático a 0,55 mg/L (rango bajo). Magnesio eritrocitario bajo. Vitamina D a 19 ng/mL. Ferritina a 25 ng/mL. Nadie le había prescrito este análisis. Su endocrinólogo vigilaba la TSH, su ginecólogo proponía un tratamiento hormonal sustitutivo. Ninguno de los dos observaba los cofactores.
El zinc en primer lugar. Cofactor de la conversión T4 a T3, cofactor de la delta-6-desaturasa (que convierte los omega-3 en prostaglandinas antiinflamatorias), modulador inmunitario. Según el Dr Claeys, más del 90% de los pacientes tiroideos están deficientes en zinc. Y Curtay confirma que el 100% de las mujeres en edad reproductiva no cubren sus necesidades por la alimentación. Zinc bisglicinato, 15 a 25 mg por día, alejado de las comidas ricas en hierro y calcio.
El magnesio después. Anti-estrés, miorelaxante, cofactor de más de 300 reacciones enzimáticas. El 80% de las mujeres están deficientes según el estudio de Val-de-Marne. El magnesio sostiene las glándulas suprarrenales (menos robo de pregnenolona), relaja el músculo uterino, y participa en la conversión T4 a T3. Magnesio bisglicinato o malato, 300 a 400 mg por día, en dos tomas.
La vitamina B6 como forma P5P (piridoxal-5-fosfato, la forma activa). Cofactor de la delta-6-desaturasa, cofactor de la detoxificación hepática de los estrógenos en fase II, cofactor de la síntesis de progesterona y de serotonina. La píldora consume B6, los estrógenos en exceso consumen B6, y sin B6, ni la conversión de los omega-3 ni la detoxificación de los estrógenos se realizan correctamente. P5P, 50 mg por día.
El selenio: cofactor de la 5’-desyodasa (conversión T4 a T3), cofactor de la glutatión peroxidasa (antioxidante tiroideo mayor). Selenometionina, 100 a 200 microgramos por día. Indispensable antes de cualquier suplementación de yodo, especialmente en caso de Hashimoto.
Los omega-3 EPA y DHA: precursores de las prostaglandinas antiinflamatorias PGE3 y de las resolvinas. El EPA es el precursor directo de las PGE3 que relajan el músculo uterino y reducen la inflamación. Aceite de pescado o microalgas, 2 a 3 g por día.
La vitamina D3: inmunomoduladora, antiinflamatoria. El estudio ENNS muestra que más del 80% de la población francesa está en insuficiencia. Objetivo sanguíneo: 60 ng/mL. Vitamina D3, 2.000 a 4.000 UI por día, con vitamina K2-MK7.
El hierro, pero solo después del dosaje de la ferritina. Objetivo: 50 a 90 ng/mL. El hierro libre es pro-oxidante (reacción de Fenton). Curtay advierte: hierro más vitamina C en suplemento genera radicales hidroxilo. Preferir la asociación hierro, magnesio y polifenoles. Nunca suplementar a ciegas.
Finalmente, la B9 como forma 5-MTHF (y nunca ácido fólico de síntesis) para apoyar la metilación hepática y la detoxificación de los estrógenos. El objetivo de homocisteína es menor o igual a 7 mg/L. Por encima, la metilación es insuficiente, y los estrógenos se estancan.
Para la suplementación, [Sunday Natural](https://sundaynat.me/


Laisser un commentaire
Sois le premier à commenter cet article.