Thomas a cinquante-deux ans. Il mange bio, fait du sport trois fois par semaine, ne fume pas, boit modérément. Depuis deux ans, il prend un complément antioxydant acheté en pharmacie : vitamine C, vitamine E, bêta-carotène, le trio classique vendu à des millions d’exemplaires avec la promesse de « lutter contre le vieillissement ». Deux ans plus tard, Thomas est toujours fatigué. Ses articulations sont douloureuses au réveil. Sa peau a perdu de son éclat. Ses bilans sanguins classiques sont normaux. Et quand je lui ai prescrit un bilan oxydatif complet, le résultat a été un choc : sa SOD érythrocytaire était effondrée, sa glutathion peroxydase était basse, son sélénium était à 65 µg/L (objectif > 100), et son glutathion réduit était au plancher. Thomas prenait des antioxydants depuis deux ans, et pourtant son organisme était en plein stress oxydant.
Le paradoxe de Thomas illustre une erreur fondamentale que le Pr Vincent Castronovo, MD PhD, professeur à l’université de Liège et enseignant au DU de Micronutrition, démonte dans son cours sur l’énergie et le stress oxydant. Prendre des antioxydants exogènes quand les défenses endogènes sont effondrées, c’est comme repeindre une façade dont les fondations s’effondrent. Le problème de Thomas n’était pas un manque de vitamine C. C’était un déficit en sélénium, en zinc et en cofacteurs du glutathion qui empêchait ses enzymes antioxydantes de fonctionner.
« Notre organisme se défend de l’activité destructrice des radicaux libres grâce à des systèmes antioxydants sûrs et efficaces. Si la production de radicaux libres augmente au-delà des capacités de défenses, ou si ces dernières sont défectueuses, alors les radicaux libres vont pouvoir s’attaquer à nos propres molécules. » Pr Vincent Castronovo, DU MAPS 2020, cours #13 “Énergie et Stress Oxydant”1
Tes cellules brûlent 50 kilos d’ATP par jour
Pour comprendre le stress oxydant, il faut d’abord comprendre d’où vient l’énergie de tes cellules. Un individu brûle environ 50 kilos d’ATP par jour2. Cinquante kilos. L’ATP (adénosine triphosphate) est la monnaie énergétique universelle du vivant. Chaque contraction musculaire, chaque battement de coeur, chaque transmission nerveuse, chaque synthèse de protéine consomme de l’ATP.
Cette ATP est produite principalement dans les mitochondries, des organites cellulaires qui sont en réalité d’anciennes bactéries. Il y a 1,6 milliard d’années, elles ont inventé un système biochimique permettant d’utiliser les propriétés au départ toxiques de l’oxygène : la respiration cellulaire. Cette invention a multiplié la production d’énergie d’un facteur 18 par rapport à la fermentation anaérobie.
Nous possédons environ 3 quadrillions de mitochondries (3 000 000 000 000 000)3. Trois mille millions de millions. Le coeur, le cerveau, le foie et les muscles sont les organes les plus riches en mitochondries, car ce sont ceux qui consomment le plus d’énergie. La mitochondrie possède son propre ADN (16 569 paires de bases, transmis exclusivement par la mère), ses propres ribosomes et sa propre machinerie de synthèse protéique. C’est littéralement un organisme dans l’organisme.
La chaîne de transport des électrons, logée dans la membrane interne de la mitochondrie, est le mécanisme central de la production d’ATP. Les électrons extraits des nutriments (glucose via la glycolyse, acides gras via la bêta-oxydation) sont transportés par le NAD (dont le précurseur est la vitamine B3) et le FAD (dont le précurseur est la vitamine B2) à travers une série de complexes protéiques (complexes I à V)4. L’énergie libérée par ce transfert sert à pomper des protons (H+) dans l’espace intermembranaire, créant un gradient qui fait tourner l’ATP synthase (complexe V), la turbine moléculaire qui assemble l’ATP.
Le coenzyme Q10 est le transporteur d’électrons entre le complexe I et le complexe II. Le cytochrome C prend le relais quand l’électron a perdu une partie de son énergie. Le fer et le cuivre sont des cofacteurs essentiels des complexes I, II, III et IV. L’article sur le vieillissement cellulaire détaille en profondeur le lien entre mitochondries, énergie et vieillissement.
10 % des électrons tombent : la source du stress oxydant
Voici le point crucial. La chaîne de transport des électrons n’est pas parfaite. Environ 10 % des électrons hautement énergétiques « tombent » de la chaîne de transport avant d’atteindre l’oxygène de façon contrôlée5. Ces électrons fugitifs rencontrent l’oxygène moléculaire (O2) de façon non contrôlée et le transforment en radical superoxyde (O2•-), une espèce réactive de l’oxygène (ROS) extrêmement instable et toxique.
C’est le prix à payer pour respirer. L’oxygène est à la fois notre carburant et notre poison. Chaque respiration produit de l’énergie ET des radicaux libres. C’est un marché faustien que l’évolution a accepté il y a 1,6 milliard d’années, en échange de la puissance énergétique de la respiration aérobie.
Les radicaux libres ne viennent pas que des mitochondries. On distingue trois sources endogènes principales : la mitochondrie (source majeure), l’inflammation (activation des macrophages et des neutrophiles qui produisent des ROS pour tuer les pathogènes) et la détoxication hépatique (la phase I des cytochromes P450 génère des intermédiaires réactifs)6. Les sources exogènes incluent les UV, les radiations ionisantes, le tabac, l’alcool, les polluants atmosphériques, les pesticides et les xénobiotiques.
Les cibles des radicaux libres sont trois catégories de molécules biologiques. Les protéines sont dénaturées par oxydation de leurs groupements thiol, ce qui altère les enzymes et les récepteurs. Les lipides, en particulier les acides gras polyinsaturés des membranes cellulaires, subissent une peroxydation en chaîne qui rigidifie les membranes et perturbe le fonctionnement des mitochondries (dont la membrane interne est riche en DHA)7. L’ADN subit des cassures simple et double brin, des modifications de bases (8-OHdG) et des mutations qui s’accumulent avec l’âge et favorisent la cancérogenèse.
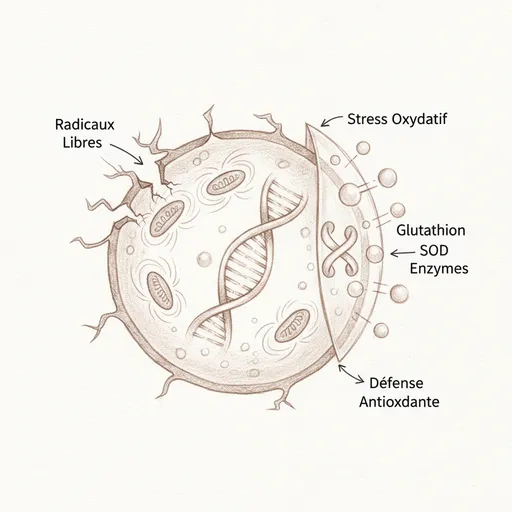
La triade de défense : SOD, GPx, catalase
Notre organisme n’est pas sans défense. Le système de défense antioxydante endogène est d’une sophistication remarquable, organisé en trois lignes8.
La première ligne est la superoxyde dismutase (SOD). Elle transforme le radical superoxyde (O2•-) en peroxyde d’hydrogène (H2O2). Il existe trois formes de SOD : la SOD1 (cuivre-zinc), localisée dans le cytoplasme, la SOD2 (manganèse), localisée dans la matrice mitochondriale, et la SOD3 (cuivre-zinc), extracellulaire. Le cuivre, le zinc et le manganèse sont donc des cofacteurs directs de la première ligne de défense antioxydante. Une carence en zinc affaiblit directement cette première barrière.
La deuxième ligne est la glutathion peroxydase (GPx). Elle transforme le peroxyde d’hydrogène (H2O2) en eau (H2O). Son cofacteur essentiel est le sélénium. Sans sélénium, la GPx ne fonctionne pas, et le H2O2 s’accumule dans la cellule. Le glutathion réduit (GSH) est le donneur d’électrons de la GPx : il est oxydé en glutathion disulfure (GSSG) au cours de la réaction, puis régénéré par la glutathion réductase (qui nécessite du NADPH, lui-même issu de la voie des pentoses phosphates)9. La catalase, présente principalement dans les peroxysomes hépatiques, constitue une voie complémentaire de dégradation du H2O2.
La catastrophe survient quand le H2O2 n’est pas neutralisé. En présence de fer ferreux (Fe2+) ou de cuivre (Cu+), le H2O2 se transforme spontanément en radical hydroxyle (OH•) par la réaction de Fenton. Et c’est là que tout bascule : nous n’avons aucun système enzymatique capable de neutraliser le radical hydroxyle10. Le radical OH• est le plus destructeur de tous les radicaux libres. C’est une bombe moléculaire qui attaque tout ce qu’elle rencontre dans un rayon de quelques nanomètres. Quand il est produit, les dégâts sont inévitables.
C’est pourquoi l’excès de fer libre est si dangereux. C’est pourquoi la ferritine doit être surveillée non seulement pour l’anémie (ferritine basse) mais aussi pour la surcharge (ferritine > 200 chez la femme, > 300 chez l’homme). C’est pourquoi le cuivre libre en excès est pro-oxydant et que le rapport cuivre/zinc doit être mesuré. Et c’est pourquoi le sélénium est probablement le micronutriment antioxydant le plus important et le plus sous-estimé.
Le sélénium : le gardien que 30 % des Français n’ont pas
Un chiffre alarmant : 30 % des Français sont en déficit de sélénium11. Trente pour cent. C’est un Français sur trois dont la glutathion peroxydase ne peut pas fonctionner correctement, dont le H2O2 s’accumule, et dont le risque de réaction de Fenton augmente.
L’étude de Brooks et al. (2001) citée dans le cours est particulièrement frappante. Publiée dans le Journal of Urology, elle montre qu’un taux plasmatique de sélénium bas avant diagnostic est associé à un risque 4 à 5 fois plus élevé de cancer de la prostate12. Les hommes du quartile le plus bas de sélénium avaient un risque multiplié par cinq par rapport à ceux du quartile le plus élevé. Le sélénium décroît significativement avec l’âge, ce qui rend la supplémentation particulièrement importante chez les hommes de plus de 50 ans.
Le sélénium n’agit pas seul. Il est cofacteur non seulement de la GPx mais aussi des thiorédoxine réductases et des iodothyronine désiodases (les enzymes qui convertissent la T4 en T3 active dans la thyroïde). Une carence en sélénium affecte donc simultanément la défense antioxydante ET la fonction thyroïdienne, ce qui explique la fréquence de l’association Hashimoto + stress oxydant.
L’acide alpha-lipoïque : l’antioxydant universel
Un antioxydant mérite le titre de « premier antioxydant des mitochondries » et d’« antioxydant universel » : l’acide alpha-lipoïque13.
L’acide alpha-lipoïque possède des propriétés uniques. Il est à la fois hydrosoluble et liposoluble, ce qui lui permet d’agir dans tous les compartiments cellulaires. Il traverse la barrière hémato-encéphalique (protégeant le système nerveux central). Il neutralise de nombreux radicaux libres différents. Et surtout, il régénère tous les autres antioxydants après qu’ils ont été oxydés : vitamine C, vitamine E, glutathion, thiorédoxine et ubiquinone (CoQ10). Sous sa forme réduite (acide dihydrolipoïque), il est le recycleur en chef du réseau antioxydant.
Il est aussi le premier cofacteur de la pyruvate décarboxylase, le complexe enzymatique qui permet l’entrée du pyruvate dans la mitochondrie (avec la vitamine B1). Sans acide alpha-lipoïque, le glucose ne peut pas être transformé en énergie mitochondriale. C’est pourquoi il est particulièrement étudié dans le diabète de type 2 et la neuropathie diabétique.
Les antioxydants exogènes : compléments, pas substituts
Les antioxydants exogènes sont des compléments des défenses endogènes, pas des substituts14.
La vitamine E (tocophérols et tocotriénols) protège les membranes cellulaires contre la peroxydation lipidique. La vitamine C protège les compartiments aqueux et régénère la vitamine E oxydée. Les caroténoïdes (bêta-carotène, lycopène, lutéine, zéaxanthine) protègent les membranes et la peau contre les UV. Le lycopène de la tomate est le caroténoïde le plus puissant grâce à sa longue chaîne de doubles liaisons conjuguées. Les polyphénols (flavonoïdes, resvératrol, curcumine, catéchines du thé vert) agissent comme antioxydants mais aussi comme modulateurs de l’expression génique via les voies NRF2 et NF-κB.
Le principe fondamental : « différents antioxydants pour différents compartiments cellulaires ». La vitamine E protège les membranes lipidiques. Le glutathion et le sélénium protègent le cytoplasme. La SOD manganèse protège la matrice mitochondriale. L’acide alpha-lipoïque traverse tous les compartiments. Prendre un seul antioxydant en espérant protéger toute la cellule, c’est mettre un seul garde devant un château qui a cent portes.
Les micronutriments mitochondriaux : la liste complète
Voici la liste complète des micronutriments nécessaires au fonctionnement mitochondrial optimal15 :
- Vitamines B1 (thiamine), B2 (riboflavine), B3 (niacine), B5 (acide pantothénique) : cofacteurs des voies de production d’ATP
- Fer et cuivre : cofacteurs des complexes de la chaîne respiratoire
- Zinc et manganèse : cofacteurs de la SOD
- Sélénium : cofacteur de la GPx
- Acide alpha-lipoïque : antioxydant mitochondrial et cofacteur de la pyruvate décarboxylase
- Coenzyme Q10 : transporteur d’électrons entre les complexes I et III
- Glutathion réduit : maître antioxydant intracellulaire
- L-carnitine : transporteur des acides gras à travers la membrane mitochondriale
- Oméga-3 (DHA) : composant essentiel de la membrane mitochondriale interne (fluidité)
- Vitamine E et vitamine C : antioxydants exogènes complémentaires
- Vitamine A : régulation de la biogenèse mitochondriale
- L-glutamine : substrat énergétique des entérocytes et des lymphocytes
L’histoire des oiseaux migrateurs illustre magnifiquement le rôle des oméga-3. Le bécasseau semipalmé (Calidris pusilla) double sa masse corporelle en deux semaines en se nourrissant de crevettes riches en EPA et DHA avant un vol direct au-dessus de l’Atlantique. Les oméga-3 s’incorporent dans les membranes de ses muscles locomoteurs, augmentent la fluidité membranaire, stimulent la biogenèse mitochondriale et améliorent la capacité aérobie16. Ce n’est pas juste de l’énergie stockée, c’est un signal métabolique qui prépare les muscles à l’endurance.
Le cercle vicieux mitochondrial
Il existe un cercle vicieux qui est au coeur de la médecine mitochondriale. Les mutations de l’ADN mitochondrial (10 fois plus fragile que l’ADN nucléaire car non protégé par des histones et doté de mécanismes de réparation archaïques) altèrent les protéines des complexes respiratoires. Les complexes défectueux laissent tomber plus d’électrons. Plus d’électrons qui tombent signifie plus de radicaux libres. Plus de radicaux libres endommagent davantage l’ADN mitochondrial. Et le cycle s’accélère avec l’âge17.
Ce cercle vicieux est impliqué dans les maladies du foie, le diabète, l’obésité, les maladies cardiovasculaires, le cancer, l’Alzheimer, l’autisme, la fatigue chronique et le vieillissement accéléré. La théorie mitochondriale du vieillissement, développée par Harman dès 1972 et confirmée par Lenaz (1999), considère les mutations somatiques de l’ADN mitochondrial induites par les radicaux libres comme la cause primaire du déclin énergétique lié à l’âge18.
Un environnement nutritionnel mitochondrial optimal est un prérequis pour préserver la santé et garantir un vieillissement harmonieux. La santé mitochondriale n’est pas un sujet de niche pour biologistes. C’est le socle de toute la santé.
Protocole naturopathique anti-stress oxydant
Voici le protocole en trois axes que j’utilise en consultation après un bilan oxydatif complet.
Axe 1 : Restaurer les défenses endogènes. C’est la priorité absolue. Sélénium 100 à 200 µg/jour (séléniométhionine). Zinc bisglycinate 15 à 25 mg/jour (cofacteur SOD1). Manganèse 2 à 5 mg/jour (cofacteur SOD2). NAC 600 à 1200 mg/jour (précurseur du glutathion). Acide alpha-lipoïque 300 à 600 mg/jour (régénérateur de tous les antioxydants). CoQ10 ubiquinol 100 à 200 mg/jour (surtout si statines, fatigue, cardiopathie). Le magnésium est un cofacteur indirect (MgATP, SOD).
Axe 2 : Apporter les antioxydants exogènes complémentaires. Vitamine C 500 à 1000 mg/jour (fractionnée en 2 prises). Vitamine E naturelle (mélange de tocophérols, pas d’alpha-tocophérol isolé) 200 à 400 UI/jour. Caroténoïdes mixtes (lycopène, lutéine, bêta-carotène naturel) via l’alimentation colorée. Polyphénols : curcumine (200 à 500 mg/jour), resvératrol, EGCG du thé vert, quercétine.
Axe 3 : Réduire les sources de radicaux libres. Limiter l’exposition aux xénobiotiques. Gérer le stress chronique (source d’inflammation et de ROS). Pratiquer une activité physique modérée (le sport à intensité modérée augmente les défenses endogènes ; le surentraînement les épuise). Traiter l’inflammation chronique de bas grade. Corriger les carences en fer (anémie) et surveiller l’excès de fer (surcharge). Privilégier la cuisson douce (la cuisson à haute température génère des produits de Maillard pro-oxydants).
Quand consulter et limites de l’approche
Thomas, après quatre mois de correction ciblée basée sur son bilan oxydatif, a vu ses marqueurs se normaliser. Son sélénium est passé de 65 à 112 µg/L. Sa GPx s’est normalisée. Son glutathion réduit est remonté. Et surtout, sa fatigue a disparu, ses douleurs articulaires ont fondu et sa vitalité est revenue. Il prend toujours des antioxydants, mais pas ceux du supermarché. Il prend du sélénium, de la NAC, de l’acide alpha-lipoïque et du CoQ10. Ses fondations sont restaurées. La façade a suivi.
Le bilan oxydatif est un outil puissant mais il nécessite un laboratoire spécialisé et une interprétation par un praticien formé. Les marqueurs doivent être interprétés ensemble, pas isolément. Un excès de SOD avec une GPx basse indique que la première ligne de défense fonctionne mais que la deuxième est défaillante (déficit en sélénium ou en glutathion). Un excès de TBARS avec des défenses normales indique une source exogène de radicaux libres (tabac, pollution, médicaments). Chaque profil est unique et la correction doit être individualisée.
La limite de cette approche est que le stress oxydant n’est jamais isolé. Il est lié à l’inflammation, à l’insulinorésistance, à la dysbiose, à la charge toxique et au stress chronique. Le bilan complet des 7 piliers de la médecine nutritionnelle est souvent nécessaire pour comprendre l’ensemble du tableau. Mais si tu devais retenir une seule chose de cet article, retiens ceci : tes cellules ont besoin de sélénium, de zinc, de glutathion et de CoQ10 pour se défendre. Pas de vitamine C en comprimé effervescent.
Pour aller plus loin
- Balance oxydative : le test du Dr Brack pour mesurer ton stress oxydant
- Balance oxydative de Marchesseau : radicaux libres, vieillissement et défenses antioxydantes
- Cancer et alimentation : ce que la micronutrition change dans l’équation
- Cholestérol et maladies cardiovasculaires : les vrais coupables que ton cardiologue ne cherche pas
Sources
Footnotes
-
Castronovo V. DU MAPS 2020, cours #13 “Métabolisme Énergétique : Stress Oxydant”. Diapositive : « Systèmes antioxydants sûrs et efficaces. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Un individu brûle environ 50 kilos d’ATP par jour. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « 3 quadrillions de mitochondries par individu. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositives : « NAD : vitamine B3 ; FAD : vitamine B2. Chaîne de transport des électrons. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « 10 % des électrons hautement énergétiques tombent de la chaîne de transport. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositives : « Radicaux libres d’origine endogène : mitochondrie, inflammation, détoxication. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Fluidité membranaire et DHA : dopage naturel chez les oiseaux migrateurs. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositives : « SOD (Cu,Zn / Mn) → GPx (Se, GSH) → Catalase. Réaction de Fenton. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Glutathion Peroxydase System. Tout déficit en sélénium provoque une accumulation de H2O2. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Nous n’avons PAS de système enzymatique pour détruire le radical OH•. Réaction de Fenton. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « 30 % des Français sont en déficit de sélénium. » ↩
-
Brooks JD et al. Plasma selenium level before diagnosis and the risk of prostate cancer development. J Urol. 2001;166(6):2034-8. Cité diapositive Castronovo. ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositives : « Acide alpha-lipoïque : The Universal Antioxidant. Régénère vitamine C, E, glutathion, thiorédoxine, ubiquinone. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Différents antioxydants pour différents compartiments cellulaires. » ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « Micronutriments mitochondriaux : liste complète. » ↩
-
Weber JM. The physiology of long-distance migration: extending the limits of endurance metabolism. J Exp Biol. 2009;212:593-597. Cité diapositive Castronovo. ↩
-
Castronovo V. DU MAPS 2020, cours #13. Diapositive : « ADN mitochondrial 10 fois plus fragile. Cercle vicieux mutations → ROS → mutations. » ↩
-
Lenaz G et al. Mitochondria, oxidative stress, and antioxidant defences. Acta Biochim Pol. 1999;46(1):1-21. Cité diapositive Castronovo. ↩

Laisser un commentaire
Sois le premier à commenter cet article.